Левин А. На пути к острову стабильности
Прошлой осенью мировую прессу облетели сообщения об абсолютно достоверном получении еще одного сверхтяжелого элемента, 118-го. Надежность этих результатов подчеркивалась отнюдь не случайно. Дело в том, что впервые такие анонсы появились гораздо раньше — в июне 1999 года. Однако позднее сотрудники американской Ливерморской лаборатории имени Лоуренса, выступившие с заявкой на это открытие, были вынуждены от нее отказаться. Выяснилось, что данные, на которых она базировалась, были сфабрикованы одним из экспериментаторов, болгарином Виктором Ниновым. В 2002 году это вызвало немалый скандал. В том же году ученые из Ливермора во главе с Кентоном Муди вместе с российскими коллегами из Объединенного института ядерных исследований в Дубне, возглавляемыми Юрием Оганесяном, возобновили эти попытки, используя другую цепочку ядерных реакций. Эксперименты были завершены лишь через три года, и вот они-то привели уже к гарантированному синтезу 118-го элемента — правда, в количестве всего лишь трех ядер. Эти результаты представлены в статье с двадцатью российскими и десятью американскими подписями, которая 9 октября 2006 года появилась в журнале Physical Review С.
О методах получения сверхтяжелых искусственных элементов и о совместной работе групп Оганесяна и Муди поговорим позже. А пока что попробуем ответить на не столь уж наивный вопрос: почему ядерные физики и химики с таким упорством ведут синтез все новых и новых элементов с трехзначными номерами в Периодической системе? Эти работы требуют сложного и дорогого оборудования и многих лет интенсивных исследований — а что в итоге? Совершенно бесполезные нестабильные экзотические ядра, которые к тому же можно пересчитать по пальцам. Конечно, специалистам интересно заниматься каждым таким ядром просто в силу его уникальности и новизны для науки — скажем, изучать его радиоактивные распады, энергетические уровни и геометрическую форму. За такие открытия подчас дают Нобелевские премии, но все же — стоит ли игра свеч? Что обещают эти исследования если не технологии, то хотя бы фундаментальной науке?
НЕМНОГО ЭЛЕМЕНТАРНОЙ ФИЗИКИ
Прежде всего напомним, что ядра всех без исключения элементов, кроме водорода, сложены из частиц двух видов — положительно заряженных протонов и не несущих электрического заряда нейтронов (ядро водорода — это единичный протон). Так что все ядра заряжены положительно, причем заряд ядра определяется числом его протонов. Это же число задает и номер элемента в Периодической системе. С первого взгляда это обстоятельство может показаться странным. Создатель этой системы Д. И. Менделеев упорядочивал элементы на основе их атомных весов и химических свойств, а об атомных ядрах наука тогда вообще не подозревала (к слову, в 1869 году, когда он открыл свой периодический закон, было известно всего лишь 63 элемента). Сейчас мы знаем (а Дмитрий Иванович узнать не успел), что химические свойства зависят от структуры электронного облака, окружающего атомное ядро. Как известно, заряды протона и электрона равны по абсолютной величине и обратны по знаку. Поскольку атом в целом электронейтрален, число электронов в точности равно числу протонов — вот искомая связь и обнаружена. Периодичность химических свойств объясняется тем, что электронное облако состоит из отдельных «слоев» — оболочек. Химические взаимодействия между атомами в первую очередь обеспечиваются электронами внешних оболочек. По мере заполнения каждой новой оболочки химические свойства получающихся элементов образуют плавный ряд, а затем емкость оболочки кончается, и начинает заполняться следующая — отсюда и периодичность. Но тут уж мы вступаем в дебри атомной физики, а она нас сегодня не интересует, нам бы успеть поговорить о ядрах.
Все встречающиеся в природе элементы имеют по несколько изотопов. Скажем, у водорода помимо основной однопротонной версии имеется тяжелая — дейтерий и сверхтяжелая — тритий (исторически сложилось так, что изотопы водорода имеют собственные названия). Ядро дейтерия состоит из протона и нейтрона, трития — из протона и двух нейтронов. Второй по счету элемент Периодической системы, гелий, имеет два природных изотопа: весьма редкий гелий-3 (два протона, один нейтрон) и куда более распространенный гелий-4 (два протона и два нейтрона). Элементы чисто лабораторного происхождения тоже, как правило, синтезируют в разных изотопных вариантах.
Отнюдь не все атомные ядра стабильны. Некоторые из них могут самопроизвольно испускать частицы и превращаться в другие нуклиды. Это явление в 1896 году открыл французский физик Антуан Анри Беккерель, который обнаружил, что уран испускает неизвестное науке проникающее излучение. Два года спустя Фредерик Кюри и его жена Мария выявили аналогичное излучение у тория, а затем открыли два нестабильных элемента, еще не вошедших в Периодическую систему — радий и полоний. Мария Кюри назвала загадочный с точки зрения тогдашней науки феномен радиоактивностью. В 1899 году англичанин Эрнест Резерфорд обнаружил, что уран испускает два вида радиации, которые он наименовал альфа- и бета-лучами. Еще через год француз Поль Виллар заметил у урана излучение третьего типа, которое тот же Резерфорд обозначил третьей буквой греческой алфавита — гамма. Позднее ученые открыли и другие виды радиоактивности.
Как альфа-, так и гамма-излучение возникает в результате внутренних перестроек ядра. Альфа-лучи — это просто потоки ядер основного изотопа гелия, гелия-4. Когда радиоактивный нуклид испускает альфа-частицу, его массовое число уменьшается на четыре единицы, а заряд — на две. В результате элемент сдвигается в таблице Менделеева на две клетки влево. Альфа-распад фактически является частным случаем целого семейства распадов, в результате которых ядро перестраивается и теряет нуклоны или группы нуклонов. Существуют распады, при которых ядро испускает единичный протон, или единичный нейтрон, или даже более массивную группу нуклонов, нежели альфа-частица (такие группы называют «тяжелыми кластерами»). А вот гамма-лучи невещественны — это электромагнитные кванты очень высокой энергии. Так что чистый гамма-распад — это, строго говоря, вообще не радиоактивность, поскольку и после него остается ядро с тем же количеством протонов и нейтронов, только находящееся в состоянии со сниженной энергией.
Бета-радиоактивность вызвана ядерными превращениями совершенно иного рода. Частицы, которые Резерфорд назвал бета-лучами, были попросту электронами, что выяснилось очень быстро, Это обстоятельство долго озадачивало ученых, поскольку все попытки найти электроны внутри ядер ни к чему не приводили. Лишь в 1934 году Энрико Ферми догадался, что бета-электроны — результат не внутриядерных перестроек, а взаимных превращений нуклонов. Бета-радиоактивность уранового ядра объясняется тем, что один из его нейтронов превращается в протон и электрон. Бывает бета-радиоактивность иного рода: протон превращается в позитрон и нейтрон (читатель заметит, что при обоих превращениях суммарный электрический заряд сохраняется). При бета-распаде также испускаются сверхлегкие и сверхпроникающие нейтральные частицы — нейтрино (точнее, позитронный бета-распад приводит к рождению собственно нейтрино, а электронный — антинейтрино). При электронном бета-распаде заряд ядра увеличивается на единицу, при позитронном, естественно, на столько же уменьшается.
Для более полного понимания бета-распада приходится копнуть еще глубже. Протоны и нейтроны считались истинно элементарными частицами лишь до середины 60-х годов прошлого века. Сейчас мы точно знаем, что те и другие состоят из троек кварков — куда менее массивных частиц, несущих положительные или отрицательные заряды. Заряд отрицательного кварка равен одной трети заряда электрона, а положительного — двум третям заряда протона. Кварки тесно спаяны друг с другом благодаря обмену особыми безмассовыми частицами — глюонами — ив свободном состоянии попросту не существуют. Так что бета-распады — это на самом деле превращения кварков.
Нуклоны внутри ядра связаны опять-таки обменными силами, переносчиками которых служат другие частицы, пионы (раньше их называли пи-мезонами). Эти связи далеко не так прочны, как глюонное склеивание кварков, именно поэтому ядра и могут распадаться. Внутриядерные силы не зависят от наличия или отсутствия заряда (следовательно, все нуклоyы реагируют друг с другом одинаково) и обладают очень коротким радиусом действия, примерно 1,4x10-15 метра. Размеры атомных ядер зависят от числа нуклонов, но в общем такого же порядка. Скажем, радиус самого тяжелого из встречающихся в природе нуклидов, урана-238, равен 7,4x10-15 метра, у более легких ядер он меньше.
С ядерным ликбезом мы покончили, перейдем к более интересным вещам. Вот для начала несколько фактов, объяснение которых открывает путь к пониманию различных механизмов нуклидного синтеза.
Факт 1.
На Земле обнаружены первые 92 элемента Периодической системы — от водорода до урана (правда, гелий был сначала открыт по спектральным линиям на Солнце, а технеций, астат, прометий и франций — получены искусственно, но позднее все они были обнаружены в земном веществе). Все элементы с большими номерами были получены искусственно, Их принято называть трансурановыми, стоящими в Периодической системе справа от урана.
Факт 3.
Соотношение между числами внутриядерных протонов и нейтронов отнюдь не произвольно. В стабильных легких ядрах их числа одинаковы или почти одинаковы — скажем, у лития 3:3, у углерода 6:6, у кальция 20:20. Но с ростом атомного номера число нейтронов растет быстрее и в самых тяжелых ядрах превышает число протонов примерно в 1,5 раза. Например, ядро стабильного изотопа висмута сложено из 83 протонов и 126 нейтронов (есть еще 13 нестабильных, у которых количество нейтронов варьирует от 119 до 132). У урана и транс-уранов отношение между нейтронами и протонами приближается к 1,6.
Факт 2.
Все элементы имеют нестабильные изотопы, встречающиеся в природе или искусственные. Например, дейтерий стабилен, а вот тритий претерпевает бета-распад, (К слову, сейчас известно около двух тысяч радиоактивных нуклидов, многие из которых применяются в различных технологиях и потому выпускаются в промышленных масштабах.) А вот стабильные изотопы есть только у первых 83 элементов таблицы Менделеева — от водорода до висмута. Девять самых тяжелых природных элементов: полоний, астат, радон, франций, радий, актиний, торий, протактиний и уран - радиоактивны во всех своих изотопных вариантах. Все без исключения трансураны также нестабильны.
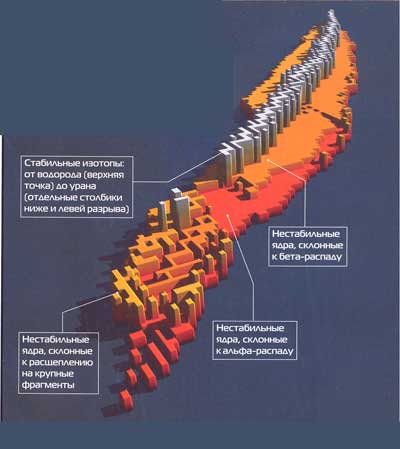
Тут-то и возникает неясность. Понятно, что ядра не могут состоять из одних протонов - их разрывали бы силы электрического отталкивания. Но нейтроны вроде бы должны увеличивать межпротонные дистанции и тем самым это отталкивание ослаблять. А ядерные силы, которые объединяют нуклоны в ядре, как уже говорилось, действуют одинаково и на протоны, и на нейтроны. Казалось бы, чем больше в ядре нейтронов, тем оно стабильней. И если это не так, то почему?
Вот объяснение «на пальцах». Ядерная материя подчиняется законам квантовой механики. Нуклоны обоих видов имеют полуцелый спин, а потому, как и все прочие такие частицы (фермионы), подчиняются принципу Паули, который запрещает одинаковым фермионам занимать одно и то же квантовое состояние. Это означает, что количество фермионов данного вида в определенном состоянии может выражаться лишь двумя числами — 0 (состояние не занято) и 1 (состояние заполнено).
В квантовой механике, в отличие от классической, все состояния дискретны. Ядро не разваливается потому, что нуклоны в нем стянуты воедино ядерными силами. Это можно наглядно представить такой картинкой — частицы сидят в колодце и просто так оттуда выскочить не могут. Физики тоже пользуются этой моделью, называя колодец потенциальной ямой. Протоны и нейтроны не одинаковы, поэтому рассаживаются в двух ямах, а не в одной. И в протонной, и в нейтронной яме имеется набор уровней энергии, которые могут занимать провалившиеся в нее частицы. Глубина каждой ямы зависит от усредненного силового взаимодействия между ее пленниками.
Теперь вспомним, что протоны взаимно отталкиваются, а нейтроны — нет. Следовательно, протоны спаяны слабее, нежели нейтроны, поэтому их потенциальная яма не так глубока. Для легких ядер это различие невелико, однако оно нарастает по мере увеличения заряда ядра. А вот энергии самых верхних непустых уровней в обеих ямах должны совпадать. Если бы верхний заполненный нейтронный уровень был выше верхнего протонного, ядро могло бы снизить свою суммарную энергию, «вынудив» занимающий его нейтрон претерпеть бета-распад и превратиться в протон. А коль скоро такое превращение было бы энергетически выгодным, оно бы со временем случилось, ядро оказалось бы нестабильным. Тот же самый финал имел бы место, если бы какой-то протон посмел превысить свой энергетический масштаб.
Вот мы и нашли объяснение. Если протонная и нейтронная ямы обладают почти равной глубиной, что характерно для легких ядер, то числа протонов и нейтронов тоже оказываются примерно одинаковыми. По мере движения вдоль таблицы Менделеева число протонов нарастает, и глубина их потенциальной ямы все более отстает от глубины нейтронного колодца. Поэтому тяжелые ядра должны иметь в своем составе больше нейтронов, нежели протонов. А вот если искусственно сделать эту разницу слишком большой (скажем, бомбардируя ядро медленными нейтронами, которые не разбивают его на осколки, а просто «приклеиваются), нейтронный уровень сильно поднимется над протонным, и ядро распадется. Эта схема, конечно, предельно упрощена, но в принципе правильна.
Пойдем дальше. Коль скоро по мере увеличения атомного номера наблюдается прогрессирующее превышение числа нейтронов над протонами, которое снижает стабильность ядер, все тяжелые нуклиды обязаны быть радиоактивными. Это и в самом деле так, не будем повторять наш Факт 2. Более того, вроде бы мы вправе предположить, что тяжелеющие нуклиды будут становиться все менее стабильными, иначе говоря, продолжительность их жизни будет постоянно снижаться. Этот вывод выглядит абсолютно логичным, но он неверен.
Начнем с того, что описанная выше схема многого не учитывает. Например, имеется так называемый эффект нуклонного спаривания. Он состоит в том, что два протона или два нейтрона могут вступить в тесный союз, образовав внутри ядра полуавтотомное состояние с нулевым угловым моментом. Члены таких пар сильнее притягиваются друг к другу, что повышает устойчивость всего ядра. Именно поэтому при прочих равных условиях наибольшую стабильность проявляют ядра с четными числами протонов и нейтронов, а наименьшую — с нечетными. Стабильность ядер зависит и от ряда других обстоятельств, слишком специальных, чтобы их здесь обсуждать.
Но главное даже не в этом. Ядро — это не просто гомогенное скопление нуклонов, хотя бы и спаренных. Многочисленные эксперименты уже давно убедили физиков, что ядро, скорее всего, обладает слоистой структурой. Согласно этой модели, внутри ядер существуют протонные и нейтронные оболочки, которые в чем-то похожи на электронные оболочки атомов. Ядра с полностью заполненными оболочками особенно устойчивы по отношению к спонтанным превращениям. Числа нейтронов и протонов, соответствующих полностью заполненным оболочкам, называются магическими. Некоторые из таких чисел надежно определены в экспериментах — это, например, 2, 8 и 20.
И вот здесь-то начинается самое интересное. Оболочечные модели позволяют вычислять магические числа сверхтяжелых ядер — правда, без полной гарантии. Во всяком случае есть все основания ожидать, что нейтронное число 184 окажется магическим. Ему могут соответствовать протонные числа 114, 120 и 126, причем последнее опять-таки должно быть магическим. Следовательно, можно предполагать, что изотопы 114-го, 120-го и 126-го элементов, содержащие по 184 нейтрона, будут жить куда дольше своих соседей. Особые надежды возлагаются на последний изотоп, поскольку он оказывается дважды магическим. Согласно наимено-вочной конвенции, о которой говорилось в первом разделе, его надо называть унбигексий-310.
Итак, можно надеяться, что существуют еще не открытые сверхтяжелые нуклиды, которые живут очень долго, во всяком случае, по меркам своего ближайшего окружения. Физики называют это гипотетическое семейство «островом стабильности». Гипотезу о его существовании впервые высказал замечательный американский физик-ядерщик (или, если угодно, химик-ядерщик) Гленн Сиборг, Нобелевский лауреат 1951 года. Он был руководителем или ключевым членом команд, создавших все девять элементов от 94-го (плутоний) до 102-го (нобелий), а также 106-й элемент, названный в его честь сиборгием.
Теперь можно ответить и на вопрос, которым заканчивается первый раздел. Синтез сверхтяжелых элементов, помимо всего прочего, шаг за шагом приближает физиков-ядерщиков к их святому Граалю — острову ядерной стабильности. Никто не может с уверенностью сказать, достижима ли эта цель, однако открытие заветного острова стало бы великим успехом науки.
114 элемент уже создан – это унунквадий. Сейчас он синтезирован в пяти изотопных версиях с числом нейтронов от 171 до 175. Как видим, до 184 нейтронов еще далеко. Однако самые стабильные изотопы унунквадия имеют период полураспада чуть меньше 3 секунд. Для 113-го элемента этот показатель составляет около половины секунды, для 115-го – менее одной десятой. Это обнадеживает.

Все искусственные элементы с 93-го до сотого были | впервые получены [ при облучении ядер | нейтронами или ядрами дейтерия ] (дейтонами). Это не 1 всегда происходило в лаборатории. Элементы 99 и 100 — эйнштейний и фермий — были впервые идентифицированы при радиохимическом анализе проб вещества, собранных в районе тихоокеанского атолла Эниветок, где 1 ноября 1952 года американцы взорвали десятимегатонный термоядерный заряд «Майк». Его оболочка была изготовлена из урана-238. Во время взрыва урановые ядра успевали поглотить до пятнадцати нейтронов, а затем претерпевали цепочки бета-распадов, которые в конечном счете и приводили к образованию изотопов этих двух элементов. Кстати, некоторые из них живут довольно долго — так, период полураспада эйнштейния-254 составляет 480 суток.
Трансфермиевые элементы с номерами более 100 синтезируются посредством бомбардировки массивных, но не слишком быстро распадающихся нуклидов тяжелыми ионами, разогнанными в специальных ускорителях. Среди лучших в мире машин этого рода — циклотроны У-400 и У-400М, принадлежащие Лаборатории ядерных реакций имени Г. М. Флерова Объединенного института ядерных исследований. На ускорителе У-400 и был синтезирован 118-й элемент, унуноктий. В таблице Менделеева он расположен в точности под радоном и, значит, должен быть благородным газом.
Впрочем, об исследовании химических свойств унуноктия говорить еще рано. В 2002 году было получено лишь одно ядро его изотопа с атомным весом 294 (118 протонов, 176 нейтронов), в 2005-м — еще два. Жили они недолго — около миллисекунды. Их изготовили посредством бомбардировки мишени из калифор-ния-249 ускоренными ионами кальция-48. Общее число кальциевых «пулек» составило 2x1019! Так что производительность унуноктиевого генератора крайне мала. Впрочем, это типичная ситуация. Зато объявленные результаты считаются вполне надежными, вероятность ошибки не превышает тысячной доли процента.
Ядра унуноктия претерпевали серию альфа-распадов, последовательно превращаясь в изотопы 116-го, 114-го и 112-го элементов. Последний, уже упоминавшийся унунбий, живет очень недолго и делится на тяжелые осколки примерно одинаковой массы.
Вот пока что и вся история. В 2007 году те же экспериментаторы надеются изготовить ядра 120-го элемента, бомбардируя плутониевую мишень ионами железа. Штурм острова стабильности продолжается.






 Издательство «Свиньин и сыновья» выпустило несколько сотен самых разных по жанру, объему и авторам, но неизменно высококультурных изданий
Издательство «Свиньин и сыновья» выпустило несколько сотен самых разных по жанру, объему и авторам, но неизменно высококультурных изданий





